La fréquence cardiaque est une variable intéressante pour suivre l’intensité d’un entraînement mais également pour suivre l’état de forme ou de fatigue. A son apparition dans la fin des années 70 (Polar Electro Oy), le cardiofréquencemètre avait pour principal objectif d’aider le sportif dans sa quête de performance. Les premiers appareils conçus étaient d’ailleurs destinés aux skieurs de fond finlandais et fonctionnaient sur le principe d’une mesure électrique cutanée en touchant l’appareil avec les doigts. Le système a très vite évolué dans les années 80 vers une mesure au niveau du thorax pour libérer les mains et permettre une activité sportive et obtenir une meilleure captation du signal électrique en provenance du nœud sinusal.

Fingertip heart rate monitor. Polar.com 1977
Aujourd’hui les cardiofréquencemètres se sont démocratisés et plus de 30 fabricants se partagent le marché qui atteindra 100 millions d’unités en 2024 selon les prévisions. La mesure et le contrôle de la fréquence cardiaque est à la fois un enjeu majeur pour la surveillance lors de la reprise d’une activité physique mais également pour contrôler l’intensité du travail ou constater sa progression.
Devant autan d’enjeux, les industriels cherchent à coller au plus proche de la demande et réduire les aspects négatifs des cardiofréquencemètres. Afin d’éviter les potentielles gènes liés à la ceinture thoracique (irritations, serrage de la cage thoracique…), les cardiofréquencemètres ont connu une mutation ces dernières années avec l’apparition de la mesure par photopléthysmographie (PPG). En 2012 MIO Alpha est la première montre grand public utilisant cette technologie.
La photopléthysmographie est une technique assez ancienne (1934-1938) qui a été intégrée dans les outils médicaux depuis la fin des années 80. L’oxymètre de pouls est l’outil les plus connu utilisant en partie cette méthode. Celle-ci consiste à pulser de la lumière dans l’organisme et analyser la modulation de la lumière renvoyée ou absorbée. Dans le cas d’un appareil type cardiofréquencemètre, la lumière est émise par des LED (vertes) vers la peau et un capteur photosensible mesure l’intensité de la lumière reflétée. La lumière traverse l’épiderme puis entre dans le derme qui possède une vascularisation avec des artérioles et des veines qui assurent l’approvisionnement et l’élimination des déchets de ces tissus.

Adapté de Seeley−Stephens Anatomy and Physiology, 6ème Edition
Lorsque la lumière rencontre un flux sanguin, les globules rouges vont refléter la lumière qui va repartir en direction du capteur photosensible placé au milieu des sources lumineuses. Ce récepteur traduit l’intensité du retour de la lumière en signal électrique pour permettre l’analyse de la modulation de lumière. L’intervalle de temps entre deux modulations correspond à une période cardiaque d’où l’on déduit la fréquence.
Différence ECG – PPG
On considère l’électrocardiogramme (ECG) comme la méthode de référence pour mesurer la fréquence cardiaque. Comparativement l’ECG et la ceinture thoracique analyse la dépolarisation du nœud sinusal alors que la technique PPG analyse le flux sanguin dans le derme à un point distant par photopléthysmographie. A chaque battement cardiaque, un volume est éjecté du cœur et envoyé dans la circulation sanguine. Ce flux pulsé depuis le cœur est entretenu par une motricité des artères à gros diamètre mais s’affaiblit en avançant surtout dans les artérioles. On retrouve une modulation significative mais la forme est moins franche que l’onde R du signal cardiaque. Ce phénomène constitue une première source d’imprécision potentielle. Également, les ceintures cardiaques mesurent pour la plupart le courant électrique de surface à une fréquence d’échantillonnage de 1kHz, ce qui indique 1000 mesures par seconde du signal électrique alors que les systèmes PPG commercialisés aujourd’hui fonctionnent entre 100 et 2000 hz. Voici encore une seconde source d’imprécision.
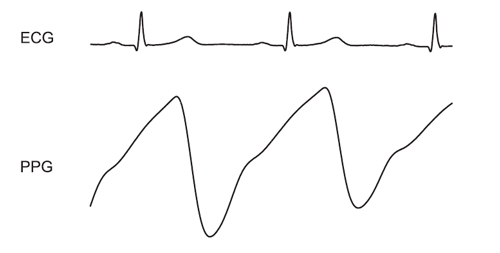
Extrait de ; John Allen. Photoplethysmography and its application in clinical physiological measurement. Physiol. Meas. 28 (2007) R1–R39
A haute fréquence le flux sanguin sera de moins en moins pulsatile et se rapprochera d’un écoulement laminaire (sans variation). A cause de cela, la mesure à haute intensité pourra ne pas être possible et certains fabricants mettent en garde contre l’utilisation dans ces zones au-delà de 160 battements par minute (bpm).
Précision de mesure
La mesure du flux sanguin va être impactée par le placement du produit pendant la mesure. Il est préférable que le produit soit plaqué contre la peau sans laisser passer de lumière pour faciliter le travail du capteur. Il peut arriver que le capteur bouge pendant l’activité et que cela entraîne une perte de signal avec des mesures très éloignées de la réalité. De plus, les mouvements et les contractions musculaires du bras vont influencer la qualité de la mesure en modifiant les variations de flux sanguin par effet de l’accélération ou simplement mobilisation du sang en amont. Il est à noter que les activités cycliques comme la course à pied sont plus simples à monitorer que des activités libres car les variations liées aux mouvements sont plus facilement filtrables par des méthodes de traitement.
Concernant l’activité, celles avec des occlusions au niveau des bras comme le CrossFit ou le tennis induisent des modulations du flux sanguins dans la zone de mesure qui ne suivent pas nécessairement celle de la fréquence cardiaque. Dans ces activités on constate une qualité de mesure médiocre comparativement à la mesure en course à pied.
Enfin, la personne mesurée peut également influencer la mesure. Les peaux mattes ou tatouées sont moins perméables à la lumière et altèrent la mesure. Également, le froid entrainera une vasoconstriction périphérique rendant plus difficile la mesure du flux sanguin.
Chaque appareil, en fonction de ces caractéristiques (fréquence de mesure, capteur, algorithme…) possède une précision intrinsèque qui s’opère ensuite sur l’individu. Il est très difficile de juger la technologie de manière générale étant donné la diversité des produits présents sur le marché.
Plus de lumière plus de précision ?
Les premiers modèles du marché (M Moi Alpha, Polar A360, Garmin, Vivo, etc…) fonctionnaient avec deux émetteurs de lumière verte placés de part et d’autre d’un récepteur photosensible. Aujourd’hui d’autres modèles sont dotés de 4, ou 6 émetteurs, mais est-ce un gage de qualité de mesure ? Sur le fond on est tenté de dire oui, plus de lumière ; plus de lumière en retour. Mais la qualité du positionnement, les mouvements ou la forme du flux sanguin restent les plus grandes contraintes pour ce type de mesure. Même si l’augmentation du nombre d’émetteurs est un plus indéniable, cela n’est pas forcément le succès garanti. Le mouvement, l’activité et la forme du flux sanguin restent les plus grands ennemis des systèmes optiques.

A gauche Mio Alpha - à droite Polar M600
PPG et fractionné ou Interval Training
Par nature, les cardiofréquencemètres optiques possèdent une latence plus importante. Il arrive que lors de séances de travail intermittent la fréquence cardiaque mesurée sur la phase d’effort tarde à monter et parfois n’arrive pas à mesurer la valeur maximale de la phase d’effort (voir graphique, zone verte). Sur les phases d’adaptation, ce retard est lié dans un premier temps à la mesure elle-même mais également au lissage des données réalisé par les fabricants afin d’éviter de montrer des valeurs aberrantes. Ce phénomène est présent sur la phase d’adaptation à l’exercice mais aussi sur les phases de récupération. L’utilisation de ces valeurs pour le calcul de délai de récupération ou d’indices similaires ne sera donc pas très judicieuse. Cette méthode de lissage permet d’améliorer la qualité des données présentées lorsque quelques battements sont manquants mais sera complètement inefficace lorsque la durée de l’interruption de signal sera plus longue (voir graphique, perte de signal).
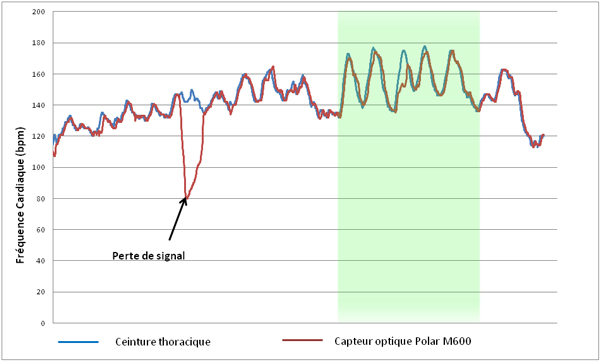
Courbes de fréquence cardiaque obtenues avec une ceinture H7 et une montre M600 à capteur optique.
Pourquoi la lumière verte et d’autres capteurs
Historiquement, les systèmes de mesure optique utilisaient des sources de lumière infrarouge. Ces dernières années les systèmes arrivés sur le marché possèdent tous des émetteurs de sources lumineuses vertes. La lumière verte possède une onde plus courte qui pénètre mieux les tissus et pourra donc avoir un retour de tissus plus profond. Plusieurs études montrent également que le comportement de la lumière verte est bien meilleur lorsque la température s’élève au-delà de 38°. Aujourd’hui certain fabricant comme polar développe des capteurs sur la base de multiples couleurs de lumière afin de pulser à plusieurs longueurs d’ondes pour augmenter la profondeur de pénétration et utilise des accéléromètres 3D pour mieux filtrer le signal en fonction des mouvements du bras. La technologie de fusion du capteurs Polar Precision Prime™ incluse dans les produits Verity sens, Vantage ou Grit X possède un capteur mesurant le signal électrique de la peau pour vérifier la qualité du contact de la montre.
PPG est variabilité de fréquence cardiaque
L’analyse de la variabilité de la fréquence cardiaque est très présente aujourd’hui dans les différents produits du marché, que cela soit directement par la restitution des valeurs de R-R ou par des index (Fitness test Polar, orthostatic, Own Zone…). Aujourd’hui la ceinture thoracique apporte une précision suffisante dans bon nombre de situations pour ce type d’analyse. En ce qui concerne les systèmes optiques, la fréquence d’échantillonnage et la précision ne sont pas suffisantes pour une utilisation de ces outils dans ce cadre. Certaines études ou validation montre des résultats similaires entre ECG et la technologie PPG, cependant il faut être attentif au contexte et protocole de mesure. Dans une situation de repos chez un athlète par exemple, la variabilité de la fréquence cardiaque sera très importante (RMSSD >80 ms). Dans ce cas le bruit de mesure lié à l’imprécision du système n’impactera pas les marqueurs temporelles, fréquentielles ou non linéaires comme une de nos études de 2019 (4). Dans notre cas, même une imprécision de meure supérieure à 30 ms n’altérera pas l’analyse. Au contraire, lors de phase d’exercice, de fatigue ou toutes autres situations entraînant une diminution de la VFC, l’imprécision impactera très fortement l’analyse de la VFC. De plus, si la mesure est de mauvaise qualité, la sensibilité de l’analyse à une variation physiologique, comme la fatigue par exemple sera très faible. Dommage, c’est précisément un des buts recherchés.
Pour finir
A la vue de l’évolution des systèmes optiques dans les dernières années et des nouveaux enjeux économiques, les solutions technologiques vont très rapidement évoluer et obtenir des précisions proches des systèmes traditionnels. Les premiers tests de nouveaux capteurs (Polar OH1, puis Verity Sens) montrent une précision largement améliorée et ouvrent la porte à de nouvelles utilisations en réduisant les contraintes du port de ceinture. Cependant, si la précision de la fréquence cardiaque est requise, qui plus est dans des zones d’intensités hautes, la ceinture thoracique offrira de bien meilleures garanties.
|
Johan Cassirame. Phd Explorateur des sciences, passionné par nature. |
Bibliographie
1. Allen, J. (2007). Photoplethysmography and its application in clinical physiological measurement. Physiological Measurement, 28(3), R1-39. https://doi.org/10.1088/0967-3334/28/3/R01
2. Arberet, S., Lemay, M., Renevey, P., Sola, J., Grossenbacher, O., Andries, D., Sartori, C., & Bertschi, M. (2013). Photoplethysmography-based ambulatory heartbeat monitoring embedded into a dedicated bracelet. Computing in Cardiology Conference (CinC), 2013, 935‑938.
3. Buchheit, M. (2014). Monitoring training status with HR measures : Do all roads lead to Rome? Frontiers in Physiology, 5. https://doi.org/10.3389/fphys.2014.00073
4. Cassirame, J., Chevrolat, S., & Mourot, L. (2019). Effects of R-R time series accuracy on heart rate variability indexes. Movement & Sport Sciences - Science & Motricité. https://doi.org/10.1051/sm/2019006
5. Delgado-Gonzalo, R., Parak, J., Tarniceriu, A., Renevey, P., Bertschi, M., & Korhonen, I. (2015). Evaluation of accuracy and reliability of PulseOn optical heart rate monitoring device. Conference Proceedings: ... Annual International Conference of the IEEE Engineering in Medicine and Biology Society. IEEE Engineering in Medicine and Biology Society. Annual Conference, 2015, 430‑433. https://doi.org/10.1109/EMBC.2015.7318391
6. Gil, E., Orini, M., Bailón, R., Vergara, J. M., Mainardi, L., & Laguna, P. (2010). Photoplethysmography pulse rate variability as a surrogate measurement of heart rate variability during non-stationary conditions. Physiological Measurement, 31(9), 1271‑1290. https://doi.org/10.1088/0967-3334/31/9/015
7. Gillinov, S., Etiwy, M., Wang, R., Blackburn, G., Phelan, D., Marc Gillinov, A., Houghtaling, P., Javadikasgari, H., & Desai, M. (2017). Variable Accuracy of Wearable Heart Rate Monitors during Aerobic Exercise. Medicine & Science in Sports & Exercise, 49, 1. https://doi.org/10.1249/MSS.0000000000001284
8. Hermand, E., Cassirame, J., Ennequin, G., & Hue, O. (2019). Validation of a Photoplethysmographic Heart Rate Monitor : Polar OH1. International Journal of Sports Medicine, 40, 462‑467. https://doi.org/10.1055/a-0875-4033
9. Horton, J., Stergiou, P., Fung, T.-S., & Katz, L. (2017). Comparison of Polar M600 Optical Heart Rate and ECG Heart Rate during Exercise. Medicine & Science in Sports & Exercise, 1. https://doi.org/10.1249/MSS.0000000000001388
10. Lin, Z., Zhang, J., Chen, Y., & Zhang, Q. (2015). Heart rate estimation using wrist-acquired photoplethysmography under different types of daily life motion artifact. 2015 IEEE International Conference on Communications (ICC), 489‑494. https://doi.org/10.1109/ICC.2015.7248369
11. Parak, J., Tarniceriu, A., Renevey, P., Bertschi, M., Delgado-Gonzalo, R., & Korhonen, I. (2015). Evaluation of the beat-to-beat detection accuracy of PulseOn wearable optical heart rate monitor. Conference Proceedings: ... Annual International Conference of the IEEE Engineering in Medicine and Biology Society. IEEE Engineering in Medicine and Biology Society. Annual Conference, 2015, 8099‑8102. https://doi.org/10.1109/EMBC.2015.7320273
12. Stahl, S. E., An, H.-S., Dinkel, D. M., Noble, J. M., & Lee, J.-M. (2016). How accurate are the wrist-based heart rate monitors during walking and running activities? Are they accurate enough? BMJ Open Sport & Exercise Medicine, 2(1), e000106. https://doi.org/10.1136/bmjsem-2015-000106
13. Sun, Y., Hu, S., Azorin-Peris, V., Kalawsky, R., & Greenwald, S. (2013). Noncontact imaging photoplethysmography to effectively access pulse rate variability. Journal of Biomedical Optics, 18(6), 061205. https://doi.org/10.1117/1.JBO.18.6.061205






















































 Comment simuler l'altitude
Comment simuler l'altitude
 Les métriques d'eye tracking pour débutants : les 4 fondamentaux à connaître
Les métriques d'eye tracking pour débutants : les 4 fondamentaux à connaître
 Capacité oxydative mitochondriale et NIRS
Capacité oxydative mitochondriale et NIRS
 Nouveauté dans la gamme GPEXE, innovations technologiques, réduction de tarifs
Nouveauté dans la gamme GPEXE, innovations technologiques, réduction de tarifs
 Profilage en sprint, force / vitesse ou charge / vitesse ?
Profilage en sprint, force / vitesse ou charge / vitesse ?
 Actualités
Actualités
 Technologie/Matériels
Technologie/Matériels
 Science
Science
 Evénements et animations
Evénements et animations



